一、铁与稀硝酸反应
稀硝酸与少量铁反应(铁粉与过量稀硝酸反应)的方程式 Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
稀硝酸与过量铁反应(过量铁粉与稀硝酸反应)的方程式 3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O
记生成物,还原产物都是NO,而铁足量则生成+2价铁,硝酸足量就是+3价铁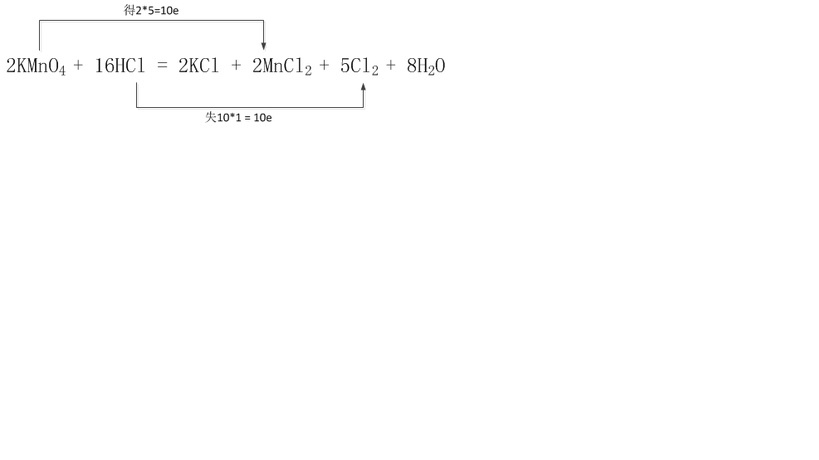
拓展资料:
铁与稀硝酸的反应与反应物的量有关,原因在于金属铁有变价。具体情况比较复杂,归纳解析如下:
一. 知识归纳
涉及的化学反应方程式:
(1)
(2)
本文来自化学自习室!
用数轴表示如下:
本文来自化学自习室!
铁与稀硝酸反应情况可以归纳为: 本文来自化学自习室!
1.
,产物仅有
,
可能有剩余;
2.
,产物仅有
,
可能有剩余;
3. ,产物为
和
的混合物。
注:在
的量比范围内,
与稀硝酸均为恰好反应,即两者恰好反应时其量比为一个范围,而不是一个比值。
将上述物质的量比换算为质量比,在应用时更加方便。与上述对应关系为:
1.
,产物仅有,
可能有剩余;
2.
,产物仅有,
可能有剩余;
3.
,产物为
和
的混合物。
应用时,先计算量比,再判断所发生的反应属于哪种情况,确定后通过计算或判断得出结论。
二、铁与硝酸的反应
1、浓硝酸过量则生成Fe(NO₃)₃,如果Fe过量,则生成Fe(NO₃)₂
Fe + 6HNO₃(浓)=加热= Fe(NO₃)₃ + 3H₂O + 3NO₂↑
Fe + 4HNO₃(浓)=加热= Fe(NO₃)₂ + 2H₂O + 2NO₂↑
2、稀硝酸也会与Fe反应得到Fe(NO₃)₃,Fe过量则有Fe(NO3)₂
Fe + 4HNO₃(稀)=== Fe(NO₃)₃ + NO↑+ 2H₂O
3Fe + 8HNO₃(稀)=== 3Fe(NO₃)₂ + 2NO↑+ 4H₂O
常温下,Fe会被浓硝酸钝化,表面形成致密的氧化膜,阻止反应继续进行。加热后,氧化膜被破坏,Fe可以与浓硝酸反应。
扩展资料:
铁的用途
1、用于制药、农药、粉末冶金、热氢发生器、凝胶推进剂、燃烧活性剂、催化剂、水清洁吸附剂、烧结活性剂、粉末冶金制品、各种机械零部件制品、硬质合金材料制品等。
2、纯铁用于制发电机和电动机的铁芯,还原铁粉用于粉末冶金,钢铁用于制造机器和工具。此外,铁及其化合物还用于制磁铁、药物、墨水、颜料、磨料等。
3、用作还原剂。用于铁盐制备。还用于制备电子元器件。
4、用作营养增补剂(铁质强化剂)。
参考资料来源:百度百科——铁
参考资料来源:百度百科——硝酸
三、铁与稀硝酸反应方程式
稀硝酸与少量铁反应(铁粉与过量稀硝酸反应)的方程式 Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
稀硝酸与过量铁反应(过量铁粉与稀硝酸反应)的方程式 3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O
记生成物,还原产物都是NO,而铁足量则生成+2价铁,硝酸足量就是+3价铁。
拓展资料:
铁与稀硝酸的反应与反应物的量有关,原因在于金属铁有变价。具体情况比较复杂,归纳解析如下:
一. 知识归纳
涉及的化学反应方程式:
(1)
(2) 本文来自化学自习室!
用数轴表示如下:
本文来自化学自习室!
铁与稀硝酸反应情况可以归纳为: 本文来自化学自习室!
1. ,产物仅有,可能有剩余;
2. ,产物仅有,可能有剩余;
3. ,产物为和的混合物。
注:在的量比范围内,与稀硝酸均为恰好反应,即两者恰好反应时其量比为一个范围,而不是一个比值。
将上述物质的量比换算为质量比,在应用时更加方便。与上述对应关系为:
1. ,产物仅有,可能有剩余;
2. ,产物仅有,可能有剩余;
3. ,产物为和的混合物。
应用时,先计算量比,再判断所发生的反应属于哪种情况,确定后通过计算或判断得出结论。
四、铁与稀硝酸的反应中氧化剂稀硝酸的物质的量与参加反应的稀硝酸物质的量为什么是1比4!!详细解答!!
Fe + 4HNO3 = Fe(NO3)3 + NO +2 H2O
从上面可以看到,NO和NO3-的比例是1比3,就是说被还原的稀硝酸和没有被还原的稀硝酸是1比3,也可以看到氧化剂稀硝酸的物质的量与参加反应的稀硝酸物质的量是1比4
其实做氧化剂的稀硝酸,N从+5价到+2价,硝酸总共有4份就是1比4
五、铁与稀硝酸反应 的化学方程式
稀硝酸与少量铁反应(铁粉与过量稀硝酸反应)的方程式 :
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
稀硝酸与过量铁反应(过量铁粉与稀硝酸反应)的方程式:
3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O
记生成物,还原产物都是NO,而铁足量则生成+2价铁,硝酸足量就是+3价铁。
扩展资料:
铁是一种金属元素,原子序数为26,铁单质化学式:Fe,平均相对原子质量为55.845。自然界中铁有四种稳定同位素Fe-54、Fe-56、Fe-57和Fe-58,不考虑质子衰变的话,可以认为半衰期无限长;另外还有两种放射性同位素Fe-55和Fe-59,半衰期分别是2.7年和44.5天。
硝酸分子式为HNO3,是一种有强氧化性、强腐蚀性的无机酸,酸酐为五氧化二氮。硝酸的酸性较硫酸和盐酸小(PKa=-1.3),易溶于水,在水中完全电离,常温下其稀溶液无色透明,浓溶液显棕色。
硝酸不稳定,易见光分解,应在棕色瓶中于阴暗处避光保存,严禁与还原剂接触。硝酸在工业上主要以氨氧化法生产,用以制造化肥、炸药、硝酸盐等。
六、铁和稀硝酸反应谁是氧化剂、还原剂、氧化产物、还原产物?
记住了 硝酸 无论是稀的还是浓度 都具有强氧化性 当然浓的氧化性更强于稀的, 所以稀硝酸肯定是氧化剂了, 铁就是还原剂.
氧化剂,被还原, 被还原成 还原产物 NO NO 就是还原产物. 还原产物也有还原性 只不过比 反应物的还原剂的还原性 弱 Fe > NO
还原剂 被氧化 被氧化成 氧化产物 Fe(NO3)3 氧化产物也有氧化性 至少弱于反应物
HNO3> Fe3+ 所以说这个反应说明3价铁的氧化性没有硝酸的强