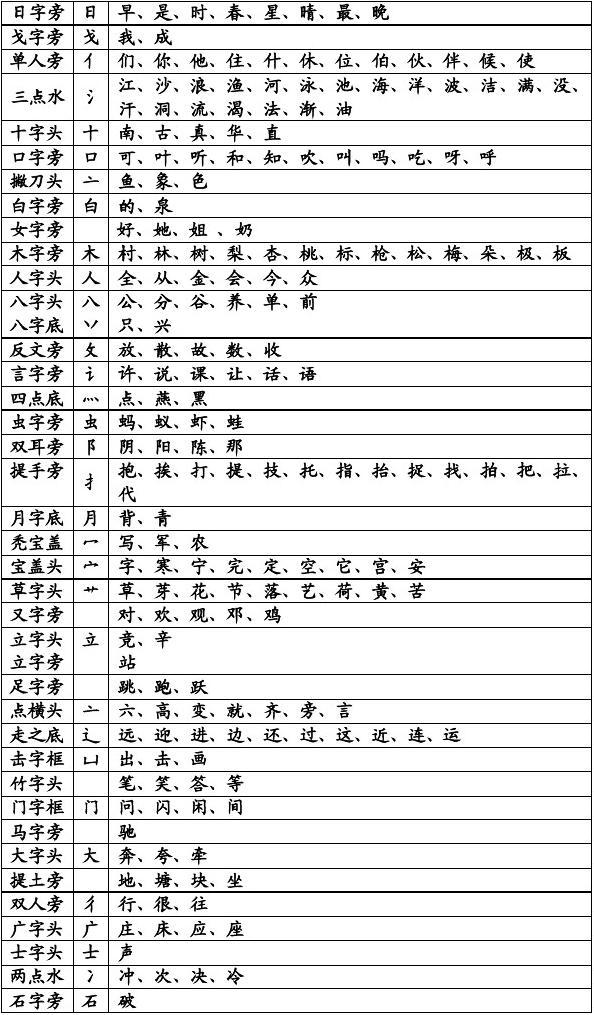
一、N2H4的结构式
N2H4的结构式:H2N-NH2,肼是两个氨基相连,在空气中能吸收水分和二氧化碳气体,并会发烟 肼和水能按任意比例互相混溶,肼也与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯。
肼和水能按任意比例互相混溶,肼也与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯。
肼的介电常数很高,液态肼的盐溶液能导电。
有强的还原性,能腐蚀玻璃、橡胶、皮革、软木等。有碱性,能与无机酸形成盐。还可以用作制药原料,如合成氨基脲、异烟肼、呋喃西林、百生肼,并用作喷气式发动机燃料、火箭燃料、显影剂、抗氧剂、还原剂等。
扩展资料:
由氢氧化钠、氯和氨或尿素用乙二醇萃取,或由无水氨与肼盐作用而制得。
储存于阴凉、通风良好的专用库房内,实行“双人收发、双人保管”制度,远离火种、热源。库温不宜超过37℃。保持容器密封,应与氧化剂、金属粉末、食用化学品分开存放,切忌混储。
采用防爆型照明、通风设施,禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
二、n2h4电子式的书写是什么?
N2H4的电子式如下:
解:肼是氮原子和氮原子形成一个共价键,剩余价键和氢原子形成共价键。
分析:首先判断化合物是离子化合物还是共价化合物;依据电子式的书写写出, 即把原子的最外层电子表示出来。
若是离子化合物,电子式由阴、阳离子的电子式组合而成,相同的离子不能合并;
若是共价化合物,电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况。
共价化合物
共价键为原子间通过共用电子对而形成的化学键。由共价键形成的化合物是共价化合物。共价化合物中原子间全部是共价键。
共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。对于不同价态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边。
三、n2h4结构式怎么写?
N2H4的结构式:H2N-NH2。
肼是两个氨基相连,在空气中能吸收水分和二氧化碳气体,并会发烟。肼和水能按任意比例互相混溶,肼也与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯。长期暴露在空气中或短时间受高温作用会爆炸分解,具有强烈的吸水性,贮存时用氮气保护并密封。
主要用途
肼是一种良好的火箭燃料,与适当的氧化剂配合,可组成比冲最高的可贮存液体推进剂。肼还可作为单元推进剂,普遍用在卫星和导弹的姿态控制上。
肼的水合物称为水合肼(N2H4·H2O),常用作锅炉水的除氧剂,是塑料、橡胶发泡剂的原料,是异烟肼等药物的原料,还用于聚酰胺和环氧树脂的制造等方面。
四、N2H4的电子式是什么
LZ好,联氨NH2-NH2又叫“肼”,可以看成是NH3分子内的一个H原子被氨基 -NH2取代的衍生物,分子结构如下图所示:
前视图 侧视图
联氨的结构类似于过氧化氢H2O2,根据联氨分子具有很大极性()这一事实,说明它是顺式结构。在N2H4中每个N原子上都有一对σ孤电子对,N的氧化数为-2。
联氨的制备方法是用次氯酸钠NaClO溶液氧化过量的NH3,总的反应:
NaClO + 2 NH3 === N2H4 + NaCl + H2O
N2H4是一种无色的高度吸湿性的可燃液体,在N2H4中N原子的孤电子对可以同H结合而显碱性,但其碱性不如NH3强,N2H4是一个二元弱碱。
N2H4和NH3一样也能生成配位化合物,例如 [Pt(NH3)2(N2H4)2]Cl2 ,
[(NO2)2Pt(N2H4)2Pt(NO2)2]等。
在碱性溶液中,N2H4是个强还原剂,它能将AgNO3还原成单质银,它也可以被卤素氧化:
N2H4+ 2 X2=== 4 HX + N2
结构图看
N2H4在空气中燃烧或与过氧化氢H2O2反应时,都能放出大量的热,因此可用作火箭燃料,做火箭的推进剂: 4245希望对你有帮助!
五、n2h4的电子式怎么写
n2h4的电子式如下图所示:
n2h4的电子式是氮原子和氮原子形成一个共价键,剩余价键和氢原子形成共价键。首先判断化合物是离子化合物还是共价化合物;依据电子式的书写写出,即把原子的最外层电子表示出来。
若是离子化合物,电子式由阴、阳离子的电子式组合而成,相同的离子不能合并;若是共价化合物,电子式由对应原子的电子式组成,并要表示出两原子之间的共用电子对情况。
肼结构式为:NH2-NH2,肼又称联氨。
无色油状液体。有类似于氨的刺鼻气味,一种强极性化合物。无色、油状液体,能很好地混溶于水、醇等极性溶剂中,具有强烈的吸水性,贮存时用氮气保护并密封。
肼的结构是从一对氨分子里各取一个氢原子然后把他们结合起来。每一个H2N-N次单元是个金字塔。H-N-H角为108°,N-N键距离1.45 ,分子符合偏转构象。旋扭难度是乙醇的两倍。结构特性像气体双氧水。